El efecto fotoeléctrico se produce cuando irradiamos con luz un metal de forma que esta consigue arrancar electrones de su superficie, tal como se muestra en la imagen.
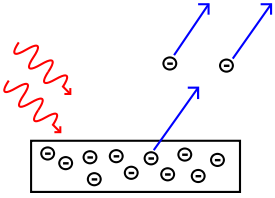
Para conseguir arrancar los electrones es necesario que la luz tenga una frecuencia (un color) mínima, llamada frecuencia de corte, que es la que consigue arrancar los primeros electrones. Según aumentamos esta frecuencia, los electrones tienen mayor energía y, por tanto, salen con mayor velocidad.

Mileva Marić (1875-1948), una brillante matemática serbia del siglo XX, estudió este fenómeno, aunque fue su marido, Albert Einstein, el que se llevó el Premio Nobel por dicho trabajo.
- En la siguiente gráfica está representada la energía (eje OY) de los electrones arrancados, en función de la frecuencia (eje OX) que tiene la luz que llega al metal.
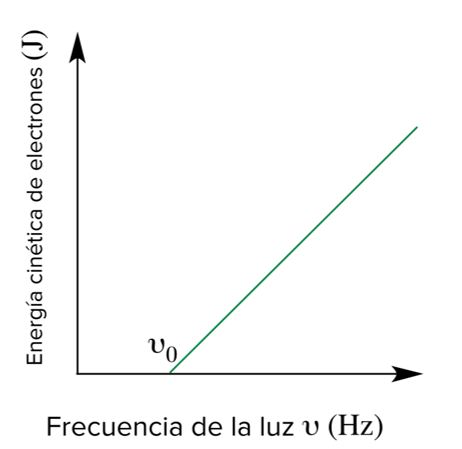
- ¿Qué tipo de función es?
- ¿La función crece o decrece?
- ¿En qué valor de frecuencia se arranca el primer electrón? ¿Con qué energía se desprende ese electrón?
- ¿Para qué valores de la frecuencia no conseguimos arrancar electrones?
- Cada metal tiene una frecuencia de corte diferente, es decir, los primeros electrones empiezan a salir a frecuencias diferentes. Para identificar el tipo de metal con el que se quiere trabajar se irradia luz cambiando la frecuencia, y cuando detectamos el primer electrón, sabemos de qué metal se trata. A continuación, se muestra una gráfica en la que aparece la función de energía de los electrones arrancados por diferentes elementos (Rubidio, Sodio, Potasio, Bario y Calcio) en función de la frecuencia radiada.
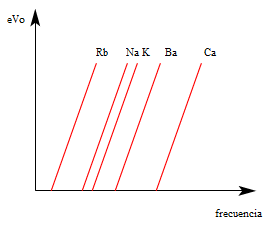
- ¿Qué metal tiene la menor frecuencia de corte? ¿Cuál tiene la mayor?
- ¿Cómo es la posición relativa de la gráfica de estas funciones?
